二酸化ケイ素
テンプレート:Redirect テンプレート:Chembox 二酸化ケイ素(にさんかけいそ、テンプレート:Lang-en)は、化学式テンプレート:Chemで表されるケイ素の酸化物で、地殻を形成する物質の一つとして重要である。シリカ(テンプレート:Lang-en[1])、無水ケイ酸、ケイ酸、酸化シリコンとも呼ばれる。純粋な二酸化ケイ素は無色透明であるが、自然界には不純物を含む有色のものも存在する。代表的なシリカ鉱物は石英(テンプレート:Lang-en、水晶)であるが、それ以外にも圧力、温度の条件等の違いにより多様な結晶相(結晶多形)が生成され、自然界では長石類に次いで産出量が多い。マグマの粘性を左右する物質でもある。鉱物以外では植物 (イネ・スギナ・サトウキビなど) にも含有され、生体内にも微量ながら含まれている。
性質
二酸化ケイ素は石英などの鉱物に代表される結晶性二酸化ケイ素と、シリカゲル・未焼成の珪藻土や生物中に存在する非結晶性 (アモルファス) 二酸化ケイ素の2つに大別される。結晶性二酸化ケイ素は共有結合結晶であり、ケイ素原子を中心とする正四面体構造が酸素原子を介して無数に連なる構造をしており、圧力や温度などの生成条件の違いにより様々な形(結晶多形)をとる。
結晶多形
二酸化ケイ素は温度や圧力をかけると結晶構造が変化する(相変態を起こす)。結晶構造などは次の一覧項で説明する。
- 温度を上昇させた時の相変化
- 常温常圧下ではα–石英が安定だが、二酸化ケイ素は温度変化によって相変化を起こす。
- 以下に示す温度は常圧での温度であり、溶剤や圧力等により変化する[2][3]。
- β–石英は高純度であればβ–トリディマイトを経由せずにβ–クリストバライトに直接相転移する[4]。
- 実際にはβ–石英を870℃以上に加熱しても、通常トリディマイトやクリストバライトに変化せず、準安定状態を保ったまま最終的に融解する[5]。これは相転移の活性化エネルギーが高いためである[注 1]。
- 上記の理由で工業的にもβ–石英の融解温度は転移温度以上に設定するが、融点未満とすることが多い (例:1550℃)。これは工業原料は粘土やアルカリといった不純物が含まれており、これらが石英の融解を補助するためである。
- 温度を下げた時の相変化
- β–トリディマイトを急速に冷却すると、114℃でα-トリディマイトとなる。
- β–クリストバライトを急速に冷却すると、270℃でα-クリストバライトとなる。
- 圧力による相変化
- 500℃から800℃、2~3 GPa以上になるとコーサイトに[6][7]、1200℃10 GPa以上でスティショバイトに転移する[8]。
- テンプレート:仮リンクは、既知の多形の中で最も高い圧力 (40 GPa) で発見されている。
自然界におけるシリカ
自然界ではケイ素は多くの場合シリカとして存在し、最も一般的に見られるのは石英である。また、砂の主成分であり、ガラスの原料となる珪砂や珪石もシリカからなる[18]。地殻内にはシリカが大量に含まれており、地球の表層の約6割がシリカを含む鉱物によって構成されているテンプレート:要出典。
天然水や水道水にも含まれており、含有量は湧水や地下水は多く、雨の混じるダム水や河川水は少ない傾向にある。また、水の味にも影響し含有量が多いほうが美味しくないと感じる傾向にある[19]。
生物学上のシリカ
生物の中には、二酸化ケイ素の形でガラス質の骨格や殻を形成するものがあり、一部のシダ植物、イネ科の植物、コケ植物などのプラント・オパールや、ケイソウ類、放散虫などの骨格、枯草菌が作る芽胞などに利用されている。また、植物一般において成長促進や環境ストレスの低減、病害虫への耐性向上の効果がある。(植物について詳しくは栄養素_(植物)#ケイ素参照)
人体中のシリカ
人体においてシリカはほとんど吸収されず、肝臓や腎臓への蓄積もほとんど行われない。水が付加したオルトケイ酸が血中に約1μg/mlの割合で吸収されるが、タンパク質とは反応せず、大部分が尿中に排泄される。[20]
食品からの摂取が困難なことから、体内のシリカ濃度は年齢を重ねると減少していく。
体内のシリカ濃度は、30代になると生まれた時に比べ半分以下になることから、シリカが加齢に関わっていると考えられている[21]。
結晶構造
| 相 | 結晶対称性 ピアソン記号, group No. |
密度, ρ g/cm3 |
注釈 | 構造 |
|---|---|---|---|---|
| α-石英 α-quartz |
三方晶系 hP9, P3121 No.152[23] |
2.648 | 鏡像異性体があり、それぞれ左右方向への3回らせん軸対称 573℃でβ-石英に変態 |

|
| β-石英 β-quartz |
六方晶系 hP18, P6222, No. 180[24] |
2.533 | 鏡像異性体があり、それぞれ左右方向への6回らせん軸対称 | 
|
| α-トリディマイト α-tridymite |
直方晶系・単斜晶系[5] oS24, C2221, No.20[25] |
2.265 | 常圧下で準安定状態 | 
|
| β-トリディマイト β-tridymite |
六方晶系 hP12, P63/mmc, No. 194[25] |
α-トリディマイトと相互に速やかに変態する β-トリディマイトは2010Kでβ-クリストバライトに変態する |

| |
| α-クリストバライト α-cristobalite |
正方晶系 tP12, P41212, No. 92[26] |
2.334 | 常圧下で準安定状態 | 
|
| β-クリストバライト β-cristobalite |
立方晶系 cF104, Fd3m, No.227[27] |
α-クリストバライトと相互に速やかに変態する 1978 Kで溶融する |
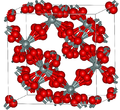
| |
| テンプレート:仮リンク | 正方晶系 tP36, P41212, No. 92[28] |
3.011 | Si5O10, Si4O14, Si8O16 環 ガラス状シリカとアルカリから600-900Kおよび40-400MPaで合成 |

|
| モガン石 | 単斜晶系 mS46, C2/c, No.15[29] |
テンプレート:Chem と テンプレート:Chemの環 | 
| |
| コーサイト | 単斜晶系 mS48, C2/c, No.15[30] |
2.911 | テンプレート:Chem と テンプレート:Chem環 900 K と3–3.5 GPaで合成 |
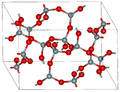
|
| スティショバイト | 正方晶系 tP6, P42/mnm, No.136[31] |
4.287 | シリカの多形体のうち最も密度の高いものの一つ ルチル型構造 7.5–8.5 GPa |

|
| テンプレート:仮リンク | 直方晶系 oP, Pbcn[32] |
4.294 | シリカの多形体のうち最も密度の高いものの一つ 40 GPaで得られる[33] |
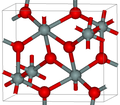
|
| テンプレート:仮リンク | 立方晶系 (cP*, P4232, No.208)[34] または 正方晶系 (P42/nbc)[35] |
2.04 | テンプレート:Chem, テンプレート:Chem 環 包摂化合物[36](青色はキセノン) 高温相のβ-メラノフログ石がある |

|
| fibrous W-silica[37] |
直方晶系 oI12, Ibam, No.72[38] |
1.97 | 硫化ケイ素の様な鎖状 | 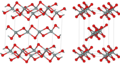
|
| テンプレート:Lang-en-short[39] | 六方晶系 | シート状の2次元構造 | 
|
反応
二酸化ケイ素はフッ化水素ガス(HF)やフッ化水素酸(HF (aq))と反応し、それぞれ四フッ化ケイ素(SiF4)、ヘキサフルオロケイ酸 (テンプレート:Chem)を生ずる。
また、固体の水酸化ナトリウム(NaOH)と熱することによりケイ酸ナトリウム(テンプレート:Chem)が生成する。ケイ酸ナトリウムに水を加えて熱すると水ガラスとなる。
利用
工業分野での利用
工業生産される二酸化ケイ素でも特に代表的なものはケイ酸をゲル化したシリカゲル(SiO2純度99.5%以上)であり、乾燥剤として食品や半導体の精密機械の保存から、消臭剤、農業肥料、建築用調湿剤などに使われる。電子材料基板やシリコンウェハーなどの研磨材などに使用されるコロイダルシリカや、耐熱器具、実験器具や光ファイバーの原料として用いられる珪砂、珪石などを溶融した後冷却し、ガラス化させた石英ガラス、樹脂の補強、研磨材、医薬品添加剤、増粘剤、農薬などの沈殿防止剤などに用いられるフュームドシリカ[40]、断熱材として用いられるシリカエアロゲルの他、エナメル、シリカセメント、陶磁器、タイヤの原料、液体クロマトグラフィー担体、電球やCRTディスプレイの表面などの表面処理剤、新聞紙の印刷インクの浸透防止など様々な分野において利用されている。陶器などの製造で石英が原材料として使用される[41]。タイヤの原料としては、沈降シリカがゴムに補強充填剤として配合される。電球に用いられる場合には、電球の内側に、眩しさを防ぎ光を拡散させる目的で塗料として塗られる[42]。
フェロシリコンの様な高温プロセスの副産物として得られるテンプレート:仮リンクはヒュームドシリカより純度が低いものの、セメントに混ぜるテンプレート:仮リンクとして利用される。また特殊な利用法として、戦車などの複合装甲として、セラミックの形で金属の間に挟んだものがある。
金属シリコンを作る際の原料としても用いられる。(炭素還元法:)[43][44]
化粧品・医薬品への添加
微粒二酸化ケイ素は一般的な粉体と比べた場合、吸水性が低い。これを利用して、アイシャドーやファウンデーションといった化粧品において湿気による固形化を防ぐ役割として使用されるほか、安定化などの目的でクリームや乳液に使用される。また硬度が高いことを利用し、歯磨き粉に研磨成分として用いられることもある。さらに医薬品においては、打錠用粉末の流動性を高めたり、錠剤の強度を高めるためのコーティング剤、軟膏・乳液の安定化のために使用されることもある。
食品添加物としての利用
食品添加物は、その吸着性を利用して、ビールや清酒、みりんといった醸造物や食用油、醤油、ソースなどのろ過工程に使われるほか、砂糖、缶詰などの製造工程にも用いられている。微粒二酸化ケイ素は吸湿・乾燥材としても使用される。とくにふりかけ等の粉形食品には、湿気による“ダマ”を防ぐ目的で添加されることがある。ただし、厚生労働省の告示の中で「母乳代替食品及び離乳食に使用してはならない」と使用基準が示されている[45]。
食品添加物として利用される非結晶性の二酸化ケイ素は、体内で消化吸収されず、その大部分が便中に排出されるため身体に影響はないが、高濃度を長期摂取した場合は有害性が示唆されている[46][47]。人体には約1.8gの微量のケイ素が存在し、こうしたケイ素はケイ酸など水溶性の化合物として食物から吸収される。
機能性原料
ケイ素は必須元素ではなくヒトを含め多くの動物の体内には殆ど蓄積しないがラットや鳥など一部の動物には必要とされ体内に蓄積される[48]。近年、げっ歯類を使ったシリカの臨床試験及び非臨床試験が行われ、糖尿病・腸内改善・コレステロールの減少・抗酸化作用などが報告されている[49][50][51]。
ろ過助剤
二酸化ケイ素の持つ多孔質や吸着能力などを利用して、ろ過用の食品添加物として使用されている。ビールをはじめとした酒類の混濁防止や調味液などのオリ下げ、ビールの泡持ち改善として使用される。こうしたろ過助剤としての二酸化ケイ素は不溶性であるためろ過過程で除去される。
埋蔵量
二酸化ケイ素(シリカ)は石英、珪砂、珪石などの形で産出する。天然の石英の資源量には限りがあるが、工業的には代わりに人工石英がもちいられる[52]。珪砂や珪石の資源量は非常に潤沢であり、工業用の純度の高いものも世界中に広く分布する[53]。
成熟した砂漠の砂にも多く含まれる。テンプレート:Main日本国内で年間200万トン以上、世界では年間1億トン以上が排出されているが、これまで未利用資源として産業廃棄物として処理されていた現状がある。最近では、SDGsの観点・グリーンケミストリーの流れから、植物で最も多くシリカを含有する籾殻より効率的にシリカを抽出し、バイオ燃料・LED・サプリメント原料・スキンケア原料・ヘアケア原料として活用する研究もなされている。
危険性
結晶質シリカ
鉱物由来に代表される結晶質シリカは、粉体状のものを多量に吸入すると塵肺の一種である珪肺の原因となる[54]。鉱石採掘現場での労働災害の事例として1930年代のホークス・ネストトンネル災害が挙げられる。石英とは別の結晶多形であるクリストバライトの粉塵に関しては国際がん研究機関 (IARC) より発がん性があるとの指摘がされていたが[55]、1997年および2012年よりヒトに対する発がん性が認められるグループ1に分類されている[56][57]。微粉末の曝露が問題であるため、結晶・粒子サイズが大きければリスクは低くなる[注 2]。
非晶質シリカ
シリカは体に有害な影響を及ぼすことがあり慢性腎臓病(CKD)など引き起こすことが示唆されている。摂取量として100mg/L以上を長期的に摂取した場合、シリカの酸化ストレスにより持続的DNA損傷により細胞死(MTTアッセイ)を誘発する、一方で80mg/L以下では体の細胞内毒素クリアランス(除去)機能により除去されたことで毒性が予防される[46]。 また、高濃度の長期摂取でシリカ結石を発症することが報告されており、三ケイ酸マグネシウムの数年間の長期服用や、10ヶ月の乳児が高濃度(172 mg Si/L)の水で粉ミルクを飲んでいたことでシリカ結石を発症したことが報告されている[47]。
低濃度では人体へ有害な影響は無いと考えられ、2004年に欧州食品安全機関(EFSA)において、食品から摂取されるケイ素化合物(二酸化ケイ素及びケイ酸塩類)について、人に対して有害影響を及ぼさない上限値は算定できないとしつつも、ケイ素換算で一日1人(60 kg 体重)当たり20~50 mgの摂取ならばヒトに対して有害影響を示さないと結論付けている[47][58]。また、日本においては、食品添加物として二酸化ケイ素を添加する場合、食品に対して2%以下とされ、母乳代用品及び離乳食への使用は禁止されている [59]。
非晶質シリカの発がん性については発がん性に関する実験動物などヒトへの影響に関する証拠が不十分として、発がん性を分類できない「グループ3」に分類されている[56][60]。
非晶質シリカは人工的に合成されるケースが多いが、自然界由来であっても植物に含まれるシリカは非晶質である。
脚注
注釈
出典
参考文献
関連項目
- ケイ酸
- ケイ酸塩(シリケート)
- ケイ酸塩鉱物
- アルミノケイ酸塩
- 鉱物 - 酸化鉱物 - 石英・鱗珪石・クリストバライト・コーサイト・スティショバイト
- 衝撃石英
- 石綿(アスベスト)
- シリカゲル
- メソポーラスシリカ
- ゼオライト
- ギンピ・ギンピ - 葉や枝に生えた毛の先端には二酸化ケイ素で出来た中空の構造物がある。
- ゾルゲル法
- モレキュラーシーブ
- アエロジル
外部リンク
テンプレート:ケイ素の化合物 テンプレート:Silica minerals テンプレート:公害 テンプレート:Normdaten テンプレート:Chem-stub
- ↑ テンプレート:Cite book
- ↑ 熱とエネルギーを科学する 171p ISBN 4501419008
- ↑ 鈴木隆夫、荒堀忠久、「ケイ石耐火物におけるトリジマイトからクリストバライトへの転移に及ぼすテンプレート:Chemの影響」『窯業協會誌』 89巻 (1981) 1036号 p.637-642, テンプレート:Doi
- ↑ テンプレート:Cite journal
- ↑ 5.0 5.1 テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite book
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ Funamori, N.; Jeanloz, R.; Miyajima N.; Fujino K. (2000). "Mineral assemblages of basalt in the lower mantle". J. Geophs. Res. - Solid Earth 105 (B11): 26037–26043. Mineral assemblages of basalt in the lower mantle Journal of geophysical research A. 2000, vol. 105, n° B11, pp. 26037-26043
- ↑ eos 306, Fall 2006, Lecture 11, The Lower Mantle
- ↑ 八木健彦、近藤忠、宮島延吉、亀卦川卓美、 テンプレート:PDFlink, PHOTON FACTORY NEWS Vol.20 No.3 p.15, NOV. 2002
- ↑ テンプレート:Cite journal First page preview
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite report
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite report
- ↑ テンプレート:Cite book
- ↑ Holleman, A. F.; Wiberg, E. (2001), Inorganic Chemistry, San Diego: Academic Press, ISBN 0-12-352651-5
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ 25.0 25.1 テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ Seifertite. Mindat.org.
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite book
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1984). Chemistry of the Elements. Oxford: Pergamon Press. pp. 393–99. ISBN 0-08-022057-6.
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ 落合満、「フュームドシリカ」『エアロゾル研究』 5巻 (1990) 1号 p.32-43, テンプレート:Doi。
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite book
- ↑ 高純度金属Siの製造方法
- ↑ 福間の無機化学の講義 三訂版 184p
- ↑ テンプレート:Cite web
- ↑ 46.0 46.1 テンプレート:Cite journal
- ↑ 47.0 47.1 47.2 テンプレート:Cite report
- ↑ テンプレート:Cite conference
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite journal
- ↑ QUARTZ CRYSTAL (INDUSTRIAL), アメリカ地質調査所
- ↑ SAND AND GRAVEL(INDUSTRIAL), アメリカ地質調査所
- ↑ テンプレート:Cite web
- ↑ 発がん物質暫定物質(2001) の提案理由日本産業衛生学会 許容濃度等に関する委員会(2001年4月6日)2018年1月13日閲覧
- ↑ 56.0 56.1 テンプレート:Cite report
- ↑ テンプレート:Cite report
- ↑ テンプレート:Cite journal
- ↑ テンプレート:Cite web
- ↑ テンプレート:Cite web
引用エラー: 「注」という名前のグループの <ref> タグがありますが、対応する <references group="注"/> タグが見つかりません